High Performance liquid Chromatography (HPLC): Pengertian, Prinsip Kerja dan Aplikasinya
A. Pengertian HPLC
HPLC atau High performance liquid chromatography adalah suatu bentuk kromatografi kolom yang memompa sampel (analit) yang dilarutkan dalam pelarut (fasa gerak) pada tekanan tinggi melalui kolom dengan bahan pengemas kromatografi terimobilisasi (fasa diam).
HPLC atau dalam Bahasa Indonesia dikenal sebagai Kromatografi Cair Kinerja Tinggi (KCKT) adalah teknik analisis yang digunakan untuk memisahkan, mengidentifikasi, dan mengukur komponen dalam suatu campuran. Kromatografi mengacu pada metode pengukuran, kromatogram mengacu pada hasil pengukuran, dan kromatograf mengacu pada instrumen. Kromatografi dapat digunakan untuk analisis kualitatif atau kuantitatif. Analisis kualitatif mengacu pada “komponen apa yang ada dalam campuran” sedangkan analisis kuantitatif mengacu pada “berapa banyak masing-masing komponen yang ada dalam campuran”
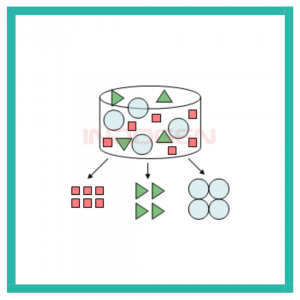
Gambar 1. Memisahkan campuran menjadi komponen
a. Sejarah Kromatografi
Metode untuk memisahkan komponen campuran meliputi filtrasi, distilasi, dan ekstraksi. Kromatografi ditemukan oleh ahli botani Rusia Mikhail Semenovich Tswett. Pada awal tahun 1900-an, Tswett mengemas kalsium karbonat dalam tabung berdiri, menempatkan pigmen yang diekstraksi dari tumbuhan di atasnya, dan kemudian menyiram tabung tersebut dengan petroleum eter sebagai pelarut (Gbr. 2).
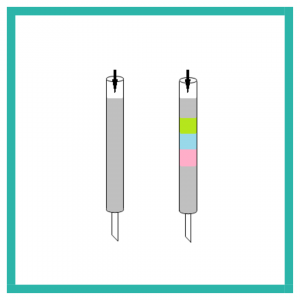
Gambar 2. Kromatograf Tswett’s
b. Mekanisme Separasi Kromatografi
Campuran ditempatkan dalam aliran cairan (petroleum eter pada Gambar 3) yang disebut fase gerak dan dipindahkan melalui media padat (bubuk kalsium karbonat pada Gambar 3) yang disebut fase diam. Komponen-komponen dalam campuran bergerak mengikuti aliran fase gerak dan berinteraksi dengan fase diam. Kecepatan geraknya bergantung pada kekuatan interaksi antara masing-masing komponen dengan fase diam. Artinya, komponen-komponen yang berinteraksi kuat dengan fasa diamnya bergerak lambat, sedangkan komponen-komponen yang berinteraksi lemah bergerak cepat, sehingga memungkinkan komponen-komponen tersebut terpisah.
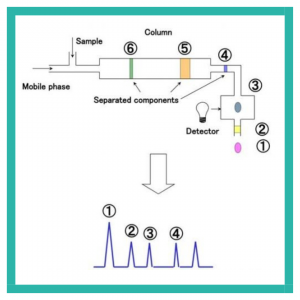
Gambar 3. Mekanisme pemisahan kromatografi (atas) dan kromatogram yang dihasilkan (bawah)
Komponen yang dipisahkan dapat dianalisis menggunakan berbagai jenis detektor. Detektor UV, misalnya, dapat mendeteksi komponen berdasarkan serapan UV. Kromatogram diperoleh dengan mengukur waktu elusi pada sumbu X dan intensitas sinyal UV pada sumbu Y. Jika kondisi pengukurannya sama, waktu elusi (posisi puncak) untuk sampel standar yang komponennya diketahui dan sampel yang tidak diketahui dapat dibandingkan untuk mengidentifikasi komponen untuk analisis kualitatif. Selain itu, karena intensitas penyerapan sebanding dengan konsentrasi, kurva kalibrasi dapat dibuat menggunakan sampel standar, dan konsentrasi komponen dapat ditentukan dengan mengukur luas atau tinggi puncak untuk analisis kuantitatif.
B. Sistem Konfigurasi HPLC
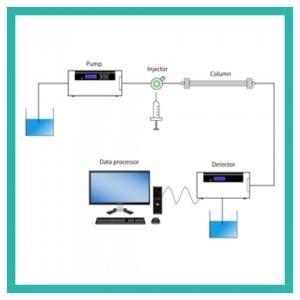
Sistem Kromatografi Cair Kinerja Tinggi (HPLC) terdiri dari lima bagian utama: pompa, injektor, kolom, detektor, dan pemroses data (Gbr. 4). Sebuah pompa, atau sistem pengiriman pelarut, menyediakan laju aliran fase gerak yang konstan di seluruh sistem HPLC. Injektor (manual), atau autosampler (otomatis), digunakan untuk memuat dan menyuntikkan sampel dalam jumlah tertentu ke dalam sistem HPLC.
Kolom memisahkan komponen campuran sampel berdasarkan interaksinya dengan fase diam dan fase gerak. Detektor mendeteksi komponen campuran sampel setelah pemisahan berdasarkan sifat fisik atau kimia tertentu dari komponen tersebut. Pemroses data mengubah dan menampilkan sinyal listrik yang terdeteksi sebagai kromatogram yang memungkinkan identifikasi dan kuantifikasi komponen sampel.
- Gambar 4. Sistem Konfigurasi HPLC
- Gambar 4. Sistem Konfigurasi HPLC 2
a. HPLC Pumps
Pompa dikelompokkan berdasarkan laju alirannya (flow rate). Berikut merupakan tipe pompa HPLC:
- Pompa nano: 1 µL/mnt atau kurang
- Pompa mikro: beberapa puluh µL/menit
- Pompa semi-mikro: beberapa ratus µL/menit
- Pompa analitik: beberapa mL/menit
- Pompa preparatif: beberapa puluh mL/menit atau lebih
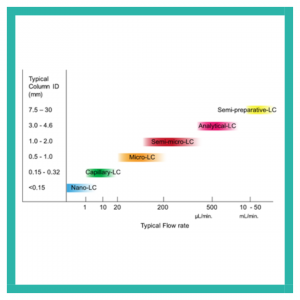
Gambar 5. Tipe Pompa Kromatografi berdasarkan laju alirannya
b. Injeksi : Manual vs Sampling Otomatis
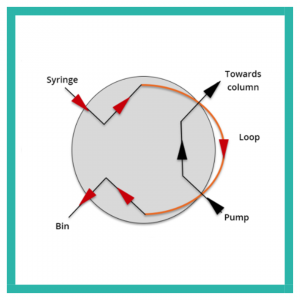
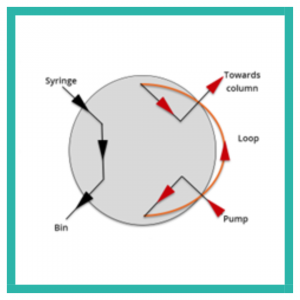
Ada dua jenis modul injektor sampel: injektor manual dan autosampler. Injektor manual mengharuskan pengguna untuk memuat dan menyuntikkan sampel melalui jarum suntik ke dalam katup injeksi pada posisi Load untuk mengisi loop sampel (Gbr. 6). Pengguna kemudian mengalihkan katup injeksi ke posisi Inject, menghubungkan loop sampel ke pompa dan kolom, memungkinkan fase gerak mengalir dari pompa melalui loop sampel ke kolom (Gbr. 7). Autosampler menggunakan katup injeksi otomatis dengan mekanisme untuk menyuntikkan beberapa sampel secara berurutan.
- Gambar 6. Posisi “Load” Katup Injeksi
- Gambar 7. Posisi “injeksi” Katup Injeksi
c. Kolom
Kolom merupakan tempat terjadinya pemisahan komponen-komponen dalam campuran sampel dan pemisahan ini bergantung pada suhu kolom. Fluktuasi suhu kolom akan mempengaruhi waktu retensi sampel, selektivitas dan bentuk puncak serta tekanan sistem. Untuk mendapatkan hasil yang dapat direproduksi, oven kolom harus digunakan untuk menjaga kolom pada suhu konstan. Oven kolom juga dapat digunakan untuk menaikkan atau menurunkan suhu kolom untuk meningkatkan pemisahan. Ketika suhu kolom meningkat, kelarutan sampel dalam fase gerak meningkat, sehingga waktu retensi lebih pendek dan waktu berjalan lebih cepat. Hal ini juga menurunkan viskositas fase gerak, yang mengakibatkan penurunan tekanan sistem, memungkinkan laju aliran fase gerak meningkat, yang juga menghasilkan waktu retensi lebih pendek dan waktu pengoperasian lebih cepat.
d. Tipe Detektor
Seperti yang ditunjukkan pada Tabel 1, terdapat berbagai detektor yang dapat digunakan bergantung pada kebutuhan aplikasi Anda dan sampel target. Detektor ultraviolet (UV) dan Photodiode Array (PDA) umumnya digunakan karena mencakup berbagai aplikasi dan komponen. Jika diperlukan sensitivitas yang lebih tinggi, detektor fluoresensi atau Spektrometer Massa (MS) dapat digunakan. Untuk deteksi yang lebih universal terhadap senyawa yang tidak menyerap, atau berfluoresensi, detektor Hamburan Cahaya Evaporatif ( Evaporative Light-Scattering Detector/ELSD) atau detektor Indeks Refraktif Diferensial (DRI) lebih tepat.
Berikut merupakan tabel yang memperlihatkan perbedaan tipe detektor dan prinsip pengukuran yang digunakan.
Tabel 1. Tipe Detektor HPLC
| Detector Type | Measurement Principle |
| UV/Visible Detector | Absorbance (AU) |
| Photodiode Array (PDA) Detector | Absorbance (AU) |
| Differential Refractive Index (RI) Detector | Refractive Index (RI) |
| Fluorescence Detector | Fluorescence |
| Electrochemical Detector | Oxidation / Reduction |
| Electrical Conductivity Detector | Conductivity |
| Mass Spectrometry Detector | Mass-to-Charge Ratio (m/z) |
| Optical Rotation Detector | Optical Rotation (OR) |
| Circular Dichroism Detector | Circular Dichroism (CD) |
| Evaporative Light Scattering Detector | Light Scattering |
C. Mode Separasi HPLC
Dalam Kromatografi Cair Kinerja Tinggi (HPLC), masing-masing komponen campuran dipisahkan menggunakan kolom berdasarkan perbedaan derajat interaksi antara komponen sampel dan fase diam kolom. Komponen yang tingkat interaksinya rendah dengan fasa diam dielusi terlebih dahulu. Interaksi tersebut meliputi adsorpsi, interaksi hidrofilik dan hidrofobik, afinitas elektron, penetrasi dan eksklusi (Gambar 8)
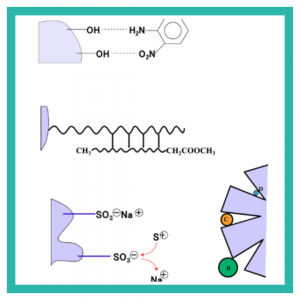
Gambar 8. Metode Separasi Kromatografi
a. Tipe Kolom dan Mode Separasi
Seperti yang ditunjukkan pada tabel di bawah (Tabel 2), terdapat berbagai jenis kolom dan mode pemisahan yang dapat digunakan, dan pilihan optimal bergantung pada sifat sampel dan analisis yang diperlukan. Ketika pelarut organik digunakan sebagai fase gerak, kolom fase normal (terutama silika gel) dapat memisahkan dan menganalisis sampel yang terdiri dari komponen yang larut dalam lemak berdasarkan adsorpsi.
Ketika komposisi pelarut air/metanol digunakan sebagai fase gerak, kolom fase terbalik/reverse-phase column (terutama rantai karbon yang terikat pada silika) dapat memisahkan dan menganalisis sampel berdasarkan interaksi hidrofobik. Kolom Kromatografi Permeasi Gel (GPC) dan Kromatografi Filtrasi Gel (GFC)
keduanya memisahkan komponen sampel berdasarkan ukuran molekulnya. Perbedaan keduanya adalah GPC menggunakan pelarut organik sebagai fase gerak sedangkan GFC menggunakan larutan air sebagai fase gerak.
Terakhir, kolom penukar ion memisahkan dan menganalisis sampel yang terdiri dari komponen ionik berdasarkan afinitas listrik.
Tabel 2. Tipe Kolom dan Mode Separasi
| Column Type | Stationary Phase | Mobile Phase | Interaction | Features |
| Normal phase | Silica gel | Organic solvent | Adsorption | Separation of fat-soluble components |
| Reversed phase | Silica C18 (ODS) | Water / MeOH | Hydrophobic | The most common method |
| GPC (Non-aqueous) | Polymer | Organic solvent | Gel permeation | Molecular weight distribution measurement |
| GFC (Aqueous) | Hydrophilic polymer | Buffer | Gel permeation | Biopolymer separation |
| Ion exchange | Ion exchanger | Buffer | Electric affinity | Separation of ionic components |
b. Perbedaan masing-masing Tipe Kolom
Fase Normal vs. Fase Terbalik
Kromatografi fase normal dan kromatografi fase balik merupakan metode pemisahan yang sangat berbeda. Dalam kromatografi fase normal, pelarut dengan polaritas rendah dilewatkan melalui kolom dengan polaritas tinggi, sehingga komponen dengan polaritas rendah dielusi terlebih dahulu. Dalam kromatografi fase terbalik, pelarut dengan polaritas tinggi dilewatkan melalui kolom non-polar, sehingga komponen dengan polaritas tinggi dielusi terlebih dahulu.
Elusi Isokratik vs. Elusi Gradien
Elusi isokratik terjadi ketika komposisi fase gerak tetap konstan selama pemisahan. Elusi gradien terjadi ketika komposisi fase gerak berubah selama pemisahan.
D. Aplikasi HPLC
HPLC telah berkembang menjadi metode yang dapat diterapkan secara universal sehingga dapat diterapkan di hampir semua bidang kimia, biokimia, dan farmasi. Informasi yang dapat diperoleh dengan metode HPLC meliputi resolusi, identifikasi dan kuantifikasi suatu senyawa. Ini juga membantu pemisahan dan pemurnian bahan kimia.
Aplikasi dari HPLC meliputi beberapa bidang di bawah ini:
- Untuk menguji kualitas obat
- Untuk mendeteksi kotoran
- Pembuatan obat-obatan farmasi
- Untuk memantau kemajuan terapi suatu penyakit
- Analisis kualitatif dan kuantitatif
- Mengevaluasi formulasi
- Memantau perubahan selama peningkatan skala
- Membantu dalam studi disolusi tablet
- Identifikasi bahan aktif
- Penentuan umur simpan
- Untuk mengontrol stabilitas obat
- Pemisahan dan pemurnian biopolimer seperti enzim atau asam nukleat
b. Aplikasi Lingkungan
- Pengujian polutan
- Deteksi senyawa fenolik dalam air minum
- Menganalisis polusi udara
- Analisis tumpahan minyak
- Menganalisis polusi plastik
c. Makanan dan Rasa
- Pemeriksaan kualitas minuman ringan dan air
- Analisis gula dalam jus buah
- Analisis pengawet
- Analisis senyawa polisiklik
- Digunakan untuk memisahkan berbagai bahan, kontaminan, dan aditif
d. Aplikasi dalam Forensik
- Identifikasi dan kuantifikasi obat
- Analisis forensik pewarna tekstil
- Penentuan kokain dan obat lain dalam darah
- Membantu menganalisis zat yang mudah menguap
- Untuk menentukan bahan yang digunakan dalam bahan peledak
e. Aplikasi dalam Uji Klinis
- Untuk menentukan obat-obatan terlarang dalam urin
- Analisis antibiotik dalam darah
- Analisis nutrisi
- Pada gangguan hati, untuk analisis bilirubin, dan biliverdin
Daftar Pustaka:
- https://jascoinc.com/ Judul Artikel: Introduction to HPLC
- https://jascoinc.com/ Judul Artikel: High-Performance Liquid Chromatography (HPLC) System Configuration
- https://jascoinc.com/ Judul Artikel: HPLC Separation Modes
- https://www.ssi.shimadzu.com/ Judul Artikel: High Performance Liquid Chromatography (HPLC) Basics